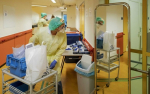
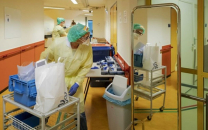
Американската биотехнолошка компанија Moderna вчера побара од регулаторите на САД итно одобрување за нејзината вакцина против COVID-19, откако целокупните резултати од спроведувањето на клиничките испитувања во доцната фаза покажаа дека е ефикасна 94,1%.

Во соопштението на Moderna се истакнува дека нејзината вакцина не предизвикува сериозни несакани ефекти. Администрацијата за храна и лекови на САД (FDA) закажа состанок на советодавниот комитет на 17 декември на кој ќе се разговара за барањето на Moderna, чија вакцина е втора вакцина со висока ефикасност што има шанса да добие зелено светло од американските регулатори за можна дистрибуција пред крајот на оваа година.
Одобрувањето на вакцината од Pfizer Inc и BioNTech SE, што се покажа 95% ефикасна во клучните испитувања, ќе биде на агендата на состанокот на надворешни експерти една недела порано. Врз основа на препораките на советничкото тело, FDA ќе донесе одлука за издавање на Овластување за итна употреба (EUA).
Moderna, која исто така најави дека ќе поднесе барање за одобрување од регулаторите во Европа, рече дека нејзината вакцина е ефективна без оглед на возраста, расата, етничката припадност и полот и дека е 100% ефикасна во спречување на тешки случаи на болеста која досега уби речиси 1,5 милиони луѓе ширум светот.
„Веруваме дека имаме вакцина со многу висока ефикасност. Сега имаме податоци што го докажуваат тоа“, изјави директорот на Moderna, Тал Закс. „Очекуваме да играме клучна улога во промената на правецот на оваа пандемија“, додаде тој.
Од вкупно 196 лица заразени со COVID-19 во студијата со повеќе од 30.000 доброволци, 185 примиле плацебо наместо вакцина. Moderna регистрирала 30 тешки случаи на болеста, сите во плацебо групата.
Вредноста на акциите на Moderna порасна за 700 проценти од почетокот на годинава.